Biofonderies: une révolution pour la recherche et l’économie mondiale
Dans le domaine en évolution rapide de la biotechnologie, les biofoundries représentent un changement transformateur dans la manière dont la recherche et le développement sont réalisés. Ces installations à la pointe de la technologie combinent automatisation, biologie synthétique et outils computationnels avancés pour accélérer le cycle de conception, de construction, de test et d’apprentissage (DBTL) des systèmes biologiques. Les biofoundries permettent l’intégration de processus biologiques complexes dans des flux de travail automatisés rationalisés, conduisant à une efficacité et une précision sans précédent dans le développement des organismes et systèmes biologiques ingénierés. Alors que nous nous trouvons aux portes d’une nouvelle ère d’innovation biotechnologique, comprendre le rôle et le potentiel des biofoundries est essentiel pour appréhender l’avenir de la science et de l’industrie.
Qu'est-ce que c'est une biofonderie?
Les biofoundries sont des installations spécialisées conçues pour rationaliser le développement de systèmes biologiques en utilisant des technologies automatisées à haut débit. Elles intègrent divers processus—tels que la synthèse d’ADN, l’édition génique, l’ingénierie des souches et l’optimisation des voies métaboliques—dans un flux de travail fluide, permettant aux chercheurs de prototyper et d’itérer rapidement des constructions biologiques. Le concept de biofoundry est analogue à celui des fonderies traditionnelles, où les matières premières sont traitées et transformées en produits finis. Cependant, dans une biofoundry, les « matières premières » sont des parties biologiques, telles que des gènes, des protéines et des voies métaboliques, et les « produits finis » sont des organismes ou des systèmes biologiques ingénierés avec des caractéristiques spécifiques et souhaitables.

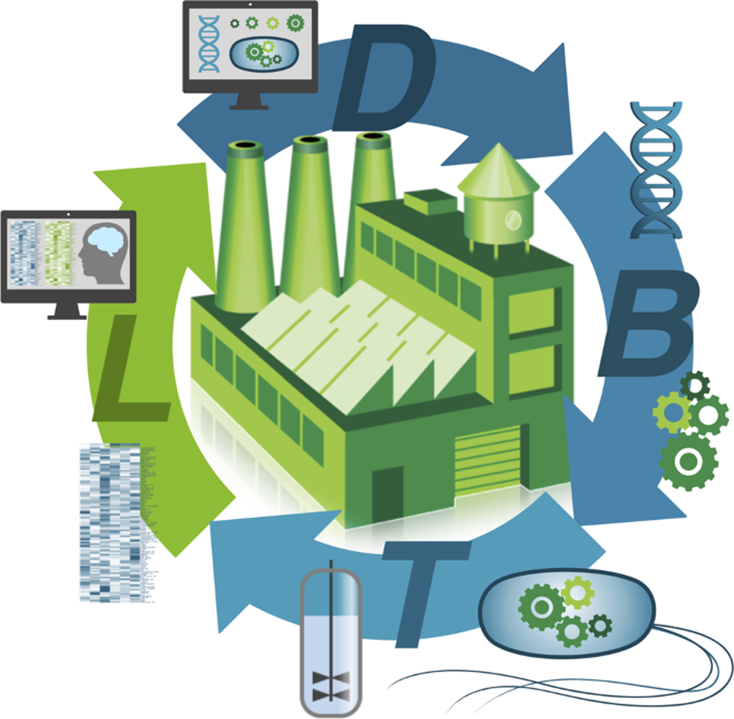
Au cœur d’une biofoundry se trouve sa capacité à exécuter le cycle DBTL de manière efficace. Ce cycle se compose des étapes suivantes :
- Conception (Design) : Utilisation d’outils computationnels pour concevoir des circuits génétiques ou des voies métaboliques.
- Construction (Build) : Construction des composants biologiques conçus à travers des techniques de synthèse et d’assemblage automatisées.
- Évaluation (Test) : Évaluation des performances des systèmes ingénierés grâce à des dépistages à haut débit.
- Apprentissage (Learn) : Analyse des données pour affiner les conceptions et améliorer les itérations suivantes.
Cette approche intégrée réduit considérablement le temps et les coûts associés à la recherche biotechnologique, ouvrant la voie à une innovation rapide dans des domaines tels que la biologie synthétique, l’ingénierie métabolique et la découverte de médicaments. En automatisant ces processus, les biofoundries améliorent la reproductibilité, l’évolutivité et la normalisation, rendant les projets complexes d’ingénierie biologique plus réalisables et efficaces.
Applications des Biofoundries dans la Recherche en Santé
Ces dernières années, les biofoundries ont apporté des contributions significatives à la recherche en santé, notamment dans les domaines du développement de vaccins, de la médecine personnalisée et de la découverte de nouveaux composés thérapeutiques. Un des exemples les plus marquants de l’impact des biofoundries sur la recherche en santé est leur rôle dans le développement rapide des vaccins contre la COVID-19. La pandémie a souligné la nécessité de solutions rapides et évolutives face aux crises sanitaires mondiales, et les biofoundries ont joué un rôle crucial pour relever ce défi.
Par exemple, le vaccin à ARN messager contre la COVID-19 a largement reposé sur les techniques de biologie synthétique facilitées par les biofoundries pour concevoir et produire rapidement les constructions d’ARN messager utilisées dans le vaccin. Cette réponse rapide a été rendue possible grâce aux flux de travail automatisés et aux capacités à haut débit des biofoundries, qui ont permis une montée en échelle rapide de la production et des tests des vaccins (Crone et al., 2020, Nature Communications ; Kitney et al., 2021, Trends in Biotechnology). Le succès de cette approche a démontré le potentiel des biofoundries à révolutionner le développement des vaccins et à répondre plus efficacement aux futures pandémies.
Les biofoundries ont également joué un rôle critique dans la découverte de nouveaux antibiotiques, en réponse à la menace croissante des bactéries résistantes aux antibiotiques. L’augmentation de la résistance aux antibiotiques est une préoccupation majeure de santé mondiale, et les biofoundries ont été essentielles dans la recherche de nouveaux composés antimicrobiens. Ces dernières années, des chercheurs ont utilisé une biofoundry pour dépister des milliers d’extraits de produits naturels à la recherche d’une activité antibiotique (Ayikpoe et al., 2022, Nature Communications ; Yuan et al., 2022, Nature Catalysis). Les systèmes automatisés ont permis l’identification rapide de plusieurs candidats prometteurs, qui sont désormais en cours de développement comme nouveaux antibiotiques potentiels. Cette capacité souligne l’importance des biofoundries pour relever l’un des défis les plus pressants de la médecine moderne.
Dans le domaine de la médecine personnalisée, les biofoundries ont le potentiel d’être utilisées pour développer des traitements spécifiques aux patients, en particulier dans l’oncologie et les maladies métaboliques. Les avancées constantes de la biologie synthétique ont permis aux scientifiques d’exploiter des cellules génétiquement modifiées, qui agissent comme des agents thérapeutiques plutôt que des petites molécules ou des biologiques traditionnels (Cubillos-Ruiz et al., 2021, Nature Reviews Drug Discovery). Ces cellules ingénierées, programmées avec des circuits génétiques synthétiques, sont capables de contrôler précisément la localisation, le moment et la posologie des activités thérapeutiques en réponse à des biomarqueurs spécifiques de la maladie. Cette technologie offre une approche révolutionnaire du traitement, en particulier pour le cancer et les troubles génétiques, car elle fournit un niveau de flexibilité, de spécificité et de prévisibilité que les thérapies conventionnelles n’ont pas. De tels avancements soulignent le potentiel des biofoundries pour accélérer le développement de ces thérapies cellulaires de pointe, qui deviennent rapidement un pilier dans la lutte contre une large gamme de maladies humaines.

Impact des Biofonderies sur les Flux de Travail de Recherche
L’intégration des biofonderies dans le flux de travail de recherche est sur le point de transformer la manière dont la recherche scientifique est menée. Les méthodes de recherche traditionnelles en biotechnologie impliquent souvent des processus laborieux et chronophages, avec une variabilité significative des résultats en raison de la nature manuelle de nombreuses procédures expérimentales. Les biofonderies répondent à ces défis en automatisant des aspects clés du processus de recherche, depuis la conception et la construction des systèmes biologiques jusqu’à leur test et leur optimisation.
L’un des impacts les plus significatifs des biofonderies sur le flux de travail de recherche est la capacité à réaliser des expériences à haut débit avec une intervention humaine minimale. En utilisant des systèmes de robotique et de gestion des liquides, les biofonderies peuvent mener simultanément des milliers d’expériences, augmentant considérablement la vitesse de génération des données. Cette capacité est particulièrement précieuse dans des domaines comme la biologie synthétique et la découverte de médicaments, où la capacité à tester et à itérer rapidement les conceptions est cruciale pour le succès.
En plus d’augmenter le débit, les biofonderies améliorent également la reproductibilité de la recherche. L’automatisation des procédures expérimentales réduit la variabilité introduite par les erreurs humaines, conduisant à des résultats plus cohérents et fiables. Cette amélioration de la reproductibilité est cruciale pour la validation des découvertes scientifiques et pour le développement de produits devant répondre à des normes réglementaires strictes. De plus, les biofonderies facilitent l’intégration des outils computationnels dans le processus de recherche. Les algorithmes d’apprentissage automatique peuvent être utilisés pour analyser les vastes quantités de données générées par les expériences à haut débit, en identifiant des motifs et en guidant la conception de nouvelles expériences. Cette combinaison d’automatisation et d’analyse des données crée une boucle de rétroaction où les résultats d’une expérience renseignent la suivante, accélérant ainsi l’ensemble du processus de recherche (Chao et al., 2017, Metabolic Engineering).
Les biofonderies permettent également la réalisation de projets de recherche plus complexes et ambitieux en fournissant une plateforme pour l’intégration de plusieurs disciplines. Par exemple, une biofonderie pourrait combiner des compétences en biologie synthétique, en bioinformatique et en ingénierie chimique pour relever un défi tel que la production de matériaux bio-basés. Cette approche interdisciplinaire est de plus en plus importante dans la recherche moderne, où la résolution de problèmes complexes nécessite souvent la collaboration d’experts de différents domaines. En facilitant ces collaborations, les biofonderies contribuent à repousser les limites de ce qui est possible en biotechnologie et dans des domaines connexes.
Biofonderies et Économie Globale dans la Quatrième Révolution Industrielle
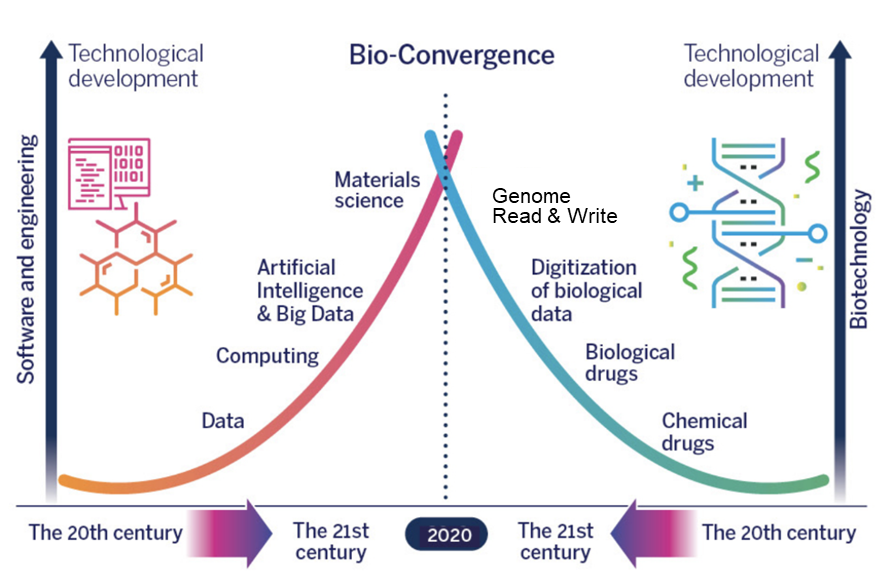
L’avènement des biofonderies représente un développement significatif dans le contexte de la Quatrième Révolution Industrielle, caractérisée par la fusion des technologies biologiques, physiques et numériques. Les biofonderies sont à l’avant-garde de cette transformation, stimulant l’innovation en biotechnologie et contribuant à l’économie mondiale de plusieurs manières.
Tout d’abord, les biofonderies devraient jouer un rôle crucial dans la bioéconomie, qui devrait connaître une croissance substantielle dans les décennies à venir. En permettant le développement et la production rapides de produits bio-basés, les biofonderies contribuent à réduire la dépendance aux combustibles fossiles et à promouvoir l’utilisation des ressources renouvelables. Ce changement a le potentiel de créer de nouvelles industries et emplois, en particulier dans des domaines tels que les produits chimiques bio-basés, l’agriculture durable et les énergies renouvelables. À titre d’exemple, la hausse des startups dans le secteur de la biologie synthétique, qui a attiré 9 milliards d’euros au cours du premier semestre 2021—plus de deux fois le montant des investissements en capital-risque de l’année précédente. Des entreprises telles qu’Amyris, Genomatica, Ginkgo Bioworks, Zymergen et OpenTrons sont désormais valorisées à plus d’un milliard de dollars chacune. De plus, divers indicateurs signalent un afflux global de plusieurs milliers de milliards de dollars dans la bioéconomie.
De plus, l’automatisation et la numérisation de la recherche biologique rendues possibles par les biofonderies devraient conduire à des réductions de coûts significatives et à des gains d’efficacité dans divers secteurs. Par exemple, dans le domaine pharmaceutique, la capacité à prototyper et à tester rapidement de nouveaux candidats médicaments pourrait réduire le temps et le coût nécessaires pour mettre de nouveaux médicaments sur le marché. Cette efficacité est non seulement bénéfique pour les entreprises impliquées, mais aussi pour l’économie mondiale, car elle pourrait conduire à des médicaments plus abordables et à des réponses plus rapides aux crises sanitaires. En outre, le potentiel des biofonderies pour démocratiser l’accès à la biotechnologie avancée est significatif, en particulier dans les pays en développement. En abaissant les barrières à l’entrée pour la recherche et la production biologiques, les biofonderies peuvent aider à niveler le terrain de jeu et permettre à davantage de pays de participer à la bioéconomie. Cette démocratisation pourrait mener à une innovation plus diversifiée, avec différentes régions apportant des solutions uniques aux défis mondiaux (Vickers et Freemont, 2022, Nature Communications).
Exemples de Biofonderies Existantes et Leurs Réalisations
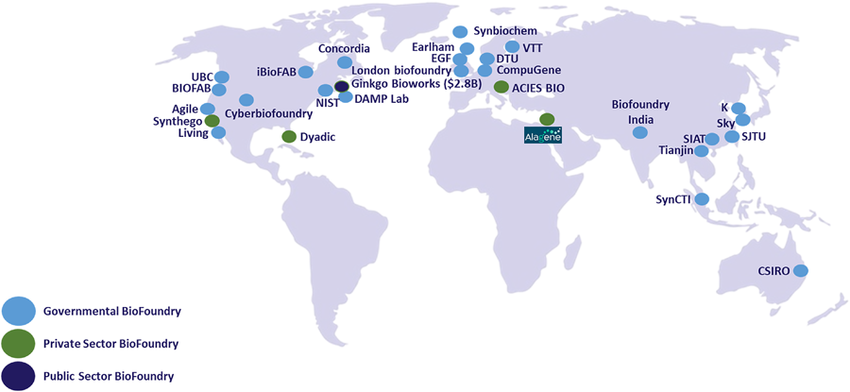
Global map of biofoundries as of 2023. Taken from : Dorfan, Y., Zeevi, A., Reinitz, G., Mualem, M., Shacham-Diamand, Y., 2023. Israel and the global synthetic biology ecosystem. Engineering Biology 7, 18–28. https://doi.org/10.1049/enb2.12027
De nombreuses biofonderies à travers le monde ont déjà apporté des contributions significatives à la biotechnologie et aux domaines connexes. Ces installations illustrent le potentiel des biofonderies pour stimuler l’innovation et relever les défis mondiaux.
L’une des biofonderies les plus emblématiques est le Joint BioEnergy Institute (JBEI) aux États-Unis, qui se concentre sur le développement de biocarburants avancés. Le JBEI a fait des progrès significatifs dans le développement de biocarburants propres et durables. En utilisant des techniques avancées en biologie moléculaire, en ingénierie chimique et en génétique, l’équipe interdisciplinaire du JBEI a conçu des microbes capables de convertir les sucres de la biomasse en biocarburants riches en énergie, tels que l’essence, le diesel et le kérosène. Ces biocarburants avancés sont conçus pour s’intégrer parfaitement aux moteurs et infrastructures existants sans compromettre les performances. Le JBEI travaille également à l’optimisation des cultures bioénergétiques, ou « matières premières, » pour améliorer leur efficacité de conversion et leur résilience environnementale. L’institut développe des méthodes plus efficaces pour décomposer la biomasse lignocellulosique en sucres fermentescibles, cruciaux pour la production de biocarburants. De plus, le JBEI réalise des essais sur le terrain pour évaluer les impacts environnementaux et économiques de ces biocarburants, avec pour objectif de satisfaire une partie significative des besoins énergétiques nationaux de manière durable.
Au Royaume-Uni, la London Biofoundry de l’Imperial College a réalisé des avancées significatives dans la biologie synthétique et la biomanufacturation. Cette installation a développé une plateforme pour le prototypage rapide de circuits génétiques, permettant l’assemblage et le test de constructions génétiques complexes en quelques jours (Hoose et al., 2023, Nature Reviews Chemistry). La Biofonderie de Londres collabore avec des entreprises pour offrir des solutions biologiques innovantes en utilisant des technologies de pointe. En collaborant étroitement avec les équipes industrielles, la Biofonderie propose une expertise en évolution dirigée, ingénierie des souches et flux de travail automatisés, facilitant le développement et la production de nouveaux produits biologiques. Ses capacités incluent la synthèse avancée d’ADN, le clonage automatisé, le dépistage à haut débit et la production en bioréacteurs à grande échelle. De plus, la Biofonderie fournit un soutien analytique complet à travers des techniques telles que la cytométrie en flux, le séquençage de nouvelle génération et l’imagerie des cellules vivantes. Ces services permettent aux entreprises d’accélérer leurs processus de R&D et de commercialiser plus efficacement les avancées biotechnologiques de pointe.
Un autre exemple est la Edinburgh Genome Foundry (EGF) en Écosse. Elle se spécialise dans l’assemblage modulaire des constructions d’ADN en utilisant des plateformes robotiques automatisées avancées, offrant un soutien étendu tant pour les projets académiques qu’industriels dans la création de thérapies personnalisées. L’EGF est à la pointe de la biologie synthétique, facilitant des projets allant de la programmation des cellules souches pour la médecine personnalisée à la mise au point de vaccins viraux et de thérapies géniques. Ses capacités incluent l’assemblage d’ADN à haut débit pour divers organismes, tels que les bactéries, les levures et les cellules mammifères, et elle fournit une gamme d’essais de phénotypage cellulaire, y compris la qPCR et la micro-fermentation à haut débit. Un outil remarquable à l’EGF est le Berkeley Lights Beacon, qui permet le clonage précis de cellules uniques et le phénotypage profond des cellules. Cette plateforme, associée aux solutions d’automatisation de l’EGF, accélère la recherche avec une exécution fiable et rentable des tâches complexes. L’EGF fournit également des logiciels de qualité industrielle pour la conception d’ADN et l’automatisation des laboratoires, améliorant l’efficacité des projets de biologie synthétique.
La Australian Genome Foundry offre des capacités avancées en conception et ingénierie des souches, particulièrement pour les modifications génétiques à grande échelle chez les levures et les bactéries. Son expertise inclut la création de bibliothèques génétiques combinatoires et le dépistage de bibliothèques de souches générées par mutagénèse chimique aléatoire. Elle utilise des technologies de fermentation à haut débit, permettant la croissance et l’analyse de centaines à des milliers de souches chaque jour, avec des options de fermentation contrôlée disponibles. La Biofonderie propose également des services sophistiqués de chimie analytique, y compris le dépistage des métabolites et des protéines, ainsi que la cytométrie en flux, le tri cellulaire et la qPCR pour le profilage de l’expression génique. De plus, elle offre une gestion de projet complète, intégrant l’ensemble du cycle Conception, Construction, Test et Apprentissage.
Toutes les biofonderies mentionnées font partie de la Global Biofoundry Alliance (GBA), une initiative qui favorise la communication entre professionnels qualifiés dans un environnement collaboratif et non compétitif pour accélérer les avancées technologiques. Composée de 35 biofonderies au moment de la rédaction de cet article, l’alliance opère avec un engagement envers l’inclusivité mondiale et l’intérêt public. La mission de la GBA est de faire avancer les technologies de biologie synthétique au bénéfice de l’humanité et de la planète, en mettant l’accent sur les projections techno-économiques comme facteur de motivation significatif, bien que non exclusif (Hillson et al., 2019, Nature Communications). La Biofonderie Bioconvergence de Paris, co-financée par le DIM BioConvS, travaille actuellement à rejoindre l’alliance. >>Voir tous les membres actuels de la GBA
Pourquoi l'Île-de-France Bénéficiera de la Création d'une Biofonderie Académique
Le paysage mondial actuel des biofonderies est caractérisé par une croissance rapide et un intérêt croissant de la part des secteurs public et privé. Les pays du monde entier reconnaissent l’importance stratégique des biofonderies pour stimuler l’innovation et maintenir leur compétitivité dans l’économie bioéconomique mondiale. Les États-Unis, le Royaume-Uni et la Chine sont parmi les leaders dans ce domaine, avec des investissements significatifs dans les infrastructures et la recherche en biofonderie.
Pour la France, le développement d’une biofonderie académique dans la région Île-de-France pourrait avoir des avantages considérables. L’Île-de-France est déjà un centre de recherche et d’innovation, avec une concentration d’universités de premier plan, d’instituts de recherche et d’entreprises de biotechnologie. L’établissement d’une biofonderie dans cette région renforcerait encore son statut de centre d’excellence en biotechnologie et en biologie synthétique.
Une biofonderie en Île-de-France offrirait aux chercheurs français un accès à des installations et des outils de pointe, leur permettant de rivaliser sur la scène mondiale. Elle attirerait également des talents et des investissements internationaux, stimulant davantage l’économie et l’écosystème d’innovation de la région. De plus, en favorisant la collaboration entre le milieu académique et l’industrie, une biofonderie pourrait contribuer à combler le fossé entre recherche et commercialisation, accélérant ainsi le développement de nouveaux produits et technologies.
C’est dans ce contexte que se développe le projet Biofonderie Paris Bioconvergence. Biofonderie distribuée avec des installations pour la synthèse d’ADN, le passage à l’échelle, les systèmes sans cellules, les souches de micro-organismes et les cellules mammifères, ce projet ambitieux est mené par les principaux experts en Biologie Synthétique en France et a bénéficié d’un financement généreux de la Région Île-de-France, ainsi que d’un co-financement considérable de toutes les institutions participantes.
Dans le contexte de la Quatrième Révolution Industrielle, l’investissement de la France dans les biofonderies positionnera le pays en tant que leader dans la bioéconomie. Alors que les défis mondiaux tels que le changement climatique et les pandémies continuent de façonner l’avenir, disposer d’une infrastructure de biofonderies solide sera crucial pour aborder ces questions à travers la biotechnologie. De plus, en réduisant la dépendance aux combustibles fossiles et en favorisant l’utilisation de ressources renouvelables, les biofonderies peuvent contribuer aux objectifs de durabilité de la France et à sa transition vers une économie plus verte, conformément à la politique France 2030.
Références
Ayikpoe, R.S., Shi, C., Battiste, A.J., Eslami, S.M., Ramesh, S., Simon, M.A., Bothwell, I.R., Lee, H., Rice, A.J., Ren, H., Tian, Q., Harris, L.A., Sarksian, R., Zhu, L., Frerk, A.M., Precord, T.W., van der Donk, W.A., Mitchell, D.A., Zhao, H., 2022. A scalable platform to discover antimicrobials of ribosomal origin. Nat Commun 13, 6135. https://doi.org/10.1038/s41467-022-33890-w
Crone, M.A., Priestman, M., Ciechonska, M., Jensen, K., Sharp, D.J., Anand, A., Randell, P., Storch, M., Freemont, P.S., 2020. A role for Biofoundries in rapid development and validation of automated SARS-CoV-2 clinical diagnostics. Nat Commun 11, 4464. https://doi.org/10.1038/s41467-020-18130-3
Cubillos-Ruiz, A., Guo, T., Sokolovska, A., Miller, P.F., Collins, J.J., Lu, T.K., Lora, J.M., 2021. Engineering living therapeutics with synthetic biology. Nat Rev Drug Discov 20, 941–960. https://doi.org/10.1038/s41573-021-00285-3
Hillson, N., Caddick, M., Cai, Y., Carrasco, J.A., Chang, M.W., Curach, N.C., Bell, D.J., Le Feuvre, R., Friedman, D.C., Fu, X., Gold, N.D., Herrgård, M.J., Holowko, M.B., Johnson, J.R., Johnson, R.A., Keasling, J.D., Kitney, R.I., Kondo, A., Liu, C., Martin, V.J.J., Menolascina, F., Ogino, C., Patron, N.J., Pavan, M., Poh, C.L., Pretorius, I.S., Rosser, S.J., Scrutton, N.S., Storch, M., Tekotte, H., Travnik, E., Vickers, C.E., Yew, W.S., Yuan, Y., Zhao, H., Freemont, P.S., 2019. Building a global alliance of biofoundries. Nat Commun 10, 2040. https://doi.org/10.1038/s41467-019-10079-2
Hoose, A., Vellacott, R., Storch, M., Freemont, P.S., Ryadnov, M.G., 2023. DNA synthesis technologies to close the gene writing gap. Nat Rev Chem 7, 144–161. https://doi.org/10.1038/s41570-022-00456-9
Kitney, R.I., Bell, J., Philp, J., 2021. Build a Sustainable Vaccines Industry with Synthetic Biology. Trends Biotechnol 39, 866–874. https://doi.org/10.1016/j.tibtech.2020.12.006
Vickers, C.E., Freemont, P.S., 2022. Pandemic preparedness: synthetic biology and publicly funded biofoundries can rapidly accelerate response time. Nat Commun 13, 453. https://doi.org/10.1038/s41467-022-28103-3
Yuan, Y., Cheng, S., Bian, G., Yan, P., Ma, Z., Dai, W., Chen, R., Fu, S., Huang, H., Chi, H., Cai, Y., Deng, Z., Liu, T., 2022. Efficient exploration of terpenoid biosynthetic gene clusters in filamentous fungi. Nat Catal 5, 277–287. https://doi.org/10.1038/s41929-022-00762-x
Avertissement : Cet article a été rédigé avec l’assistance de l’intelligence artificielle pour garantir clarté et cohérence. Veuillez noter que bien que le processus d’édition ait impliqué des outils d’IA, toutes les sources et données citées sont authentiques et ont été rigoureusement vérifiées. Le contenu reflète des informations scientifiques précises et à jour.
Action financée par la Région Île-de-France
Follow us on LinkedIn
Join our LinkedIn group
Contact: contact@bioconvs.org
Consult our data protection policy
Address:
DIM BioConvS
Faculté des Sciences - Université Paris Cité
5 rue Thomas Mann 75013 Paris


